مطالعهای روی موشها که توسط دانشمندان مرکز ملی تحقیقات قلبی عروقی (CNIC) انجام شد، نشان داد که یکی از اجزای شیر مادر سیگنالهای ضروری را فراهم میکند که باعث بلوغ متابولیسم قلب در نوزاد پس از تولد میشود و به قلب نوزاد اجازه عملکرد میدهد. به درستی و تضمین بقای پس از زایمان.
این مطالعه نشان داد که اسید چرب (FA) گاما لینولنیک اسید (GLA) شیر مادر به گیرنده رتینوئید X (RXR) موجود در سلولهای قلب – کاردیومیوسیتها – متصل میشود و بلوغ میتوکندری سلولها را تحریک میکند تا از لیپیدها برای تولید استفاده کنند. ATP. تولههایی که به دلیل کمبود RXR در سلولهای قلبشان پرورش یافته بودند، یا آنهایی که با شیر بدون GLA تغذیه میشدند، اندکی پس از تولد مردند.
دکتر مرسدس ریکوت، سرپرست گروه سیگنالینگ گیرنده هسته ای در CNIC، پیشنهاد کرد که نتایج می تواند پیامدهای درمانی قابل توجهی برای اختلالات قلبی عروقی شامل اختلال عملکرد میتوکندری و متابولیک، و همچنین برای بیماری های مرتبط با تغییرات در فرآیندهای رشد پس از تولد داشته باشد.
Ricote و تیم بین المللی محققان در مورد یافته های خود گزارش دادند طبیعت، در مقاله ای با عنوان “γ-لینولنیک اسید در شیر مادر باعث بلوغ متابولیک قلب می شود”، که در آن آنها بیان کردند، نتایج ما این ایده در حال ظهور را تقویت می کند که تعاملات مادر و نوزاد در اوایل زندگی محرک های اصلی فیزیولوژی ارگانیسم است و اهمیت شیر مادر را برجسته می کند. بلع برای بلوغ میتوکندری قلب های پری ناتال، یافته ای با پیامدهای عمده برای سلامت قلب.

قلب پستانداران برای حفظ انقباض به یک منبع انرژی مداوم نیاز دارد و کاردیومیوسیت ها چیزی را نشان می دهند که نویسندگان آن را “متابولیسم بسیار انعطاف پذیر” می نامند، به این معنی که آنها می توانند طیف گسترده ای از سوبستراها از جمله گلوکز، لیپیدها، لاکتات و اسیدهای آمینه را برای تولید این ماده مصرف کنند. ATP (آدنوزین تری فسفات) که به عنوان ارز انرژی ضروری سلول استفاده می شود.
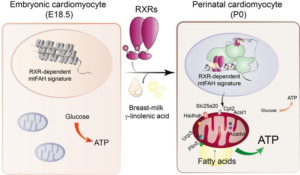
کاردیومیوسیتهای جنین عمدتاً به اکسیداسیون گلوکز و لاکتات متکی هستند، اما پس از تولد، منبع اصلی تولید ATP اکسیداسیون لیپید میتوکندری است. اگرچه این فرآیند برای بقای ارگانیسم حیاتی است، دانشمندان اطلاعات کمی در مورد سیگنال هایی که باعث سازگاری فیزیولوژیکی قلب پس از تولد می شوند، داشته اند.
محققان توضیح دادند: «به نظر میرسد تغییر قلب جنین به نوزاد به تدریج در طول دو هفته اول زندگی اتفاق میافتد و به یک محفظه عملکردی میتوکندری میرسد که در آن اسیدهای چرب بهطور مؤثری توسط β-اکسیداسیون ۷ (FAO) اکسید میشوند. اما در حالی که این مرحله تطبیقی برای حفظ ضربان قلب و بقا حیاتی است، “در مورد مکانیسمهای مولکولی و سیگنالهای بالادستی که این انتقال متابولیک را آموزش میدهند، اطلاعات بسیار کمی وجود دارد.”
مطالعه جدید روی موشها نشان میدهد که GLA موجود در شیر مادر به گیرنده رتینوئید X (RXR) موجود در کاردیومیوسیتهای نوزادان متصل میشود و باعث بلوغ میتوکندریهای سلولی میشود. RXR به عنوان یک حسگر تغذیه ای لیپیدها و مشتقات ویتامین A عمل می کند، بیان ژن را تغییر می دهد و بر عملکردهای بیولوژیکی مانند ایمنی، تمایز سلولی و متابولیسم تأثیر می گذارد. این مطالعه نشان داد که RXR پس از فعال شدن توسط GLA مادر، برنامههای ژنتیکی را آغاز میکند که میتوکندری سلولها را با آنزیمها و پروتئینهای دیگری که برای شروع مصرف لیپیدها، منبع اولیه انرژی در قلب بالغ، نیاز دارند، مجهز میکند.
مطالعات نشان داد که در مدلهای موشی که در آنها ژنهای RXR در قلب جنینی حذف شده بود (حیوانات EDKO)، فقدان RXR در سلولهای قلب مانع از تولید صحیح انرژی میتوکندری در قلب حیوانات تازه متولد شده میشد. نارسایی شدید قلبی و مرگ اندکی پس از تولد. این تیم نوشت: «… 80 درصد از تولههای EDKO در 24 ساعت اول زندگی مردند و هیچ نوزاد EDKO بیش از روز 7 پس از تولد زنده نماند.
به طور مشابه، موشهای نوزادی نوع وحشی که با شیر مادرانی که از رژیم غذایی بدون چربی (FFD) تغذیه میکردند، ظرف 48 ساعت پس از تولد مردند. نتایج ترکیبی از مطالعات آنها نشان داد که شیر-FA از سازگاری متابولیک در قلب نوزاد پشتیبانی می کند، “… و نشان می دهد که فعال شدن یک محور شیر-FA-RXR یک مکانیسم مرتبط برای حفظ زندگی پری ناتال است.”
آزمایشهای آزمایشگاهی بعدی GLA را بهعنوان لیگاند RXR شناسایی کرد و آزمایشهای بیشتر روی موشها نشان داد که نوزادان مادرانی که رژیم غذایی بدون چربی داشتند، زمانی که شیرشان با GLA تکمیل میشد، رشد میکردند. به طور قابلتوجهی، نوزادانی که توسط مادرانی که از رژیم غذایی معمولی تغذیه میکردند نیز در اثر مکیدن شیر FFD مردهاند، این محققین “نقش شیر مادر و نه رسوبات چربی در دوران بارداری، به عنوان منبع GLA مربوطه برای اطمینان از بقای پری ناتال را حمایت میکند.” بیشتر اشاره کرد.
یافته های ترکیبی این مطالعه نشان می دهد که اسید چرب GLA موجود در شیر مادر، سیگنال کلیدی است که عملکرد صحیح قلب را پس از تولد تضمین می کند. GLA پروتئین سلولی RXR را فعال می کند، که سپس تغییرات هماهنگ بیان ژن را هدایت می کند تا اطمینان حاصل شود که میتوکندری های کاردیومیوسیت بالغ می شوند تا بتوانند در محیط خارج رحمی انرژی تولید کنند.
ریکوت توضیح داد: «نیاز به حفظ یک ضربان ثابت و بدون وقفه، نیاز انرژی بسیار زیادی را به قلب تحمیل می کند. کاردیومیوسیتها برای تامین انرژی مورد نیاز خود، کنترل دقیقی بر مسیرهای سلولی تولید انرژی دارند. هر گونه عدم تعادل در این مکانیسم های انرژی زیستی می تواند منجر به ایجاد آسیب شناسی های قلبی عروقی جدی شود.
برای Ricote، بخشی از تازگی این مطالعه «در نشان دادن این است که RXR برخلاف آنچه قبلاً تصور می شد، نقش مهمی در عضله قلب بازی می کند. این یک پیشرفت مفهومی مهم در زمینه گیرنده های هسته ای است.
به گفته نویسنده اول آنا پاردس، دکترا، این مطالعه چارچوب جدیدی را برای درک سازگاری های پس از زایمان که در پستانداران تازه متولد شده برای برآورده کردن الزامات محیط خارج رحمی رخ می دهد، ارائه می دهد. پاردس توضیح داد: “تولد یک چالش فیزیولوژیکی برای نوزاد است.” با این مطالعه، ما نشان میدهیم که شیر مادر، علاوه بر عملکرد تغذیهایاش، با دستور دادن به کاردیومیوسیتها که نیاز به فعال کردن متابولیسم خود دارند، نقش سیگنالدهندهای نیز ایفا میکند، زیرا دیگر توسط فیزیولوژی مادر پشتیبانی نمیشوند.
نتایج راه را برای درمان هایی برای تعدیل فعالیت RXR در قلب با داروهای خاص باز می کند، از جمله برخی که قبلاً تأییدیه FDA را برای درمان سرطان دارند. Ricote نتیجه گرفت: “مطالعه ما RXR را به عنوان یک هدف درمانی احتمالی برای اختلالات قلبی نوزادان و بیماری های سیستمیک ناشی از خطاهای متابولیک پیشنهاد می کند.” و از نقطه نظر تغذیه، این تیم اظهار داشت: «فراوانی کم GLA در شیر مادر انسان با کمبود رشد در نوزادان مرتبط است، که نشان دهنده نقش بالقوه این اسید چرب در فیزیولوژی نوزادان انسان است.»